2022はサンバイオにとって、「承認」の年になるだろう確信が世の中にはあったと思う。「世界初の再生細胞薬」しかも「大量生産できる他家細胞」しかも「将来的に脳梗塞等他疾患にも適応見込み十分に有り」の希望がもうすぐそこにまで迫っていた。ところがそうはならなかった。今年のサンバイオを一文字で表すのなら「耐」だろうか。振り返ってみようと思う。(大納会今日の終値788円。)
1月
特記事項なし
2月
今後、1カ月程度で「承認申請」 を行う見込みだと発表し、「先駆け総合評価相談」の終了と「承認申請」の準備開始についてIR。加えて、750万株(14.5%希薄化、77億円獲得)のMSワラント(増資)を発表した。大手企業も遅延を繰り返すほど、難しいと言われる新薬の承認申請。化合物の場合だけれど医薬品の開発には10年以上の時間と数百億~数千億円規模の費用が必要と言われ、成功確率は年々低下(10年前:1/1.6万→現在:1/2.5万=0.004%)し、難易度が上昇している。そんな世界で、世界初の再生細胞薬を申請まで持ち込んだサンバイオの力量というのを、自分はやはり買う。
3月
「国内SB623慢性期外傷性脳損傷プログラム製造販売承認申請の完了について」を発表した。思えば、2018年11月に治験成功を発表。2019年には申請かと匂わせていたが、2022までかかった。後出しで思えば、3年間かかったことは今にして思えば妥当なラインか。会社が早々に期待を市場に持たせすぎた感は否めないが、大手企業も難しい申請をよくやってくれた。3.7に承認申請完了をIRし3.11に決算説明会を行った。この時の森社長談「現在力強く上市準備をしまして、この一つ一つがですね当社のノウハウ・基盤になって参りますので、これを日本から世界中にベストプラクティスを展開していこうと考えております。」「日本での申請が最も重要なところでありまして、これを通して当社としましては確固たる基盤ができてきたところと考えておりますのでこの基盤を最大限に生かしてこの企業価値最大化に努めていく所存であります。」「(バイオテクの会社は日本では千社以上、グローバルでは数千、数万社以上あるが承認申請・上市に至る会社はほんの一握りだということに触れた上で)新しい再生細胞薬と言う領域で承認申請までこぎつけたこと、そして承認・上市までが目前に迫っていると言う所まできたと言う事は非常に大きな意義があることだと思っておりまして、会社としては新たなステージに入ってきたなと感じております。」いや、ほんとその通りで、かっこいい。
申請完了IR後、材料出尽くしか、ワラントか、ウクライナ情勢の懸念もあってかで株価は下落をし、3.7終値1957円→3.11終値1526円になった。
4月
アナリスト・機関投資家向け説明会が4.13に開催され、説明会資料および説明会音声が当日の夜23時頃にアップされた。ANN学会の報告が興奮気味に森社長からあった。4月27日の株主総会は、申請完了ということもあって、明るい総会になった。(詳しくは、本ブログ過去記事参照http://bouchan.info/archives/32645336.html)
5月
R-SAT(再生医療等製品の管理システム)の特許取得。戦略担当執行役員にアンドリュー・リュウ(Andrew Liu)氏が就任(IRは6月1日)。生産部長に中田圭三氏が就任。就職するというのは、人生の大きな出来事で、多くの方が人生を賭けて入社するというのは応援団としても希望が持てる。
6月
ワラント中
7月
750万株のMSワラントが終わり。重しが取れたと思いきや、「国内SB623慢性期外傷性脳損傷プログラム製造販売承認取得の状況について」というIRで8月の当局での議題に上がらない=9月までの承認申請はないことが判明。
8月
人事異動で澤口 和美 信頼性保証・薬事部長→執行役員 信頼性保証・薬事部長に。平田 晋也 事業部副事業部長→執行役員 研究開発本部長に。承認に向けた社内体制の改善だと読む。
9月
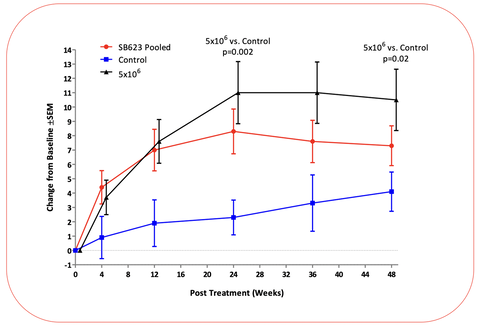
決算説明会。いまだに48週有意差なしの話を出す人がいるが、世界の権威マカリスター先生が学会で報告したのは、「250万細胞・500万細胞・1000万細胞」一括としてのデータ(24週有意差ありでも、48週有意差なし)ではなく、「500万細胞」オンリーのデータ(グラフの黒線)で、効果は抜群(添付写真参照)。この時はお代わり増資はないと思っていたのに、10月に増資することになるorz。
10月
「国内SB623慢性期外傷性脳損傷プログラム製造販売承認取得の状況について(続報)」というIRで、「生産関連の審査に対する当社の従前からの対応がより具体化し、まだ時間を要すことが判ったため、当社としては、今期中の承認取得は無いものと判断しています。」と発表。そしてその1週間後、まさかのお代わり増資(900万株 15.1%希薄化 90億円調達)発表。今年最大の苦しい月となった。
11月
慶應義塾大学医学部と、SB623のアルツハイマー型認知症を対象とした共同研究に関する契約を締結。サンバイオは大学との締結は過去幾度となくやっており、自分の中では現段階ではスルーIR。ただ、創業科学者岡野先生のいらっしゃる大学なので、岡野先生の意中を知りたいとは思う。
12月
四半期決算短信にて、円安もあって経営利益まさかの4億3700万円の黒字(初めて?)。「再生医療等製品の包装・表示・保管に関する自社施設の設置及び業許可の取得に関するお知らせ」と「第14回世界脳損傷学会(The 14th World Congress on Brain Injury)における口頭発表演題採択のお知らせ」が立て続けに出る。東京本社の聖路加タワーをどのようにしているのか、何フロア賃貸契約しているのか、その辺りを次回の株主総会で聞いてみたい。できれば社内の風景写真なんかを公表してもらいたい。
承認は遅れているが、その他のこと(上市後準備や学会発表等等)は進んでいる。承認さえなされれば、サンバイオはバイオベンチャー企業→再生細胞薬製造販売企業に転換する。日本での上市実績を持って、他国がどう反応するか。例えば中国はTBI患者1100万人。アメリカはTBI患者551万人で国防総省もSB623に興味を示している。他国の出方も楽しみだ。長期的に見ればGPIF始め、巨大投資機関が買いに走る時期も承認を得れればいずれ来るだろう。まずは「承認」。それしかない。2023こそ承認を得なければ。
今までサンバイオはいくつもの壁を乗り越えてきた。
イノベーションを起こそうとする姿勢を応援する。
今まで築いてきた実績は必ず日本の宝になる。
2023は、きっと承認を迎えるだろう。
期待しかない。
がんばれサンバイオ!!



